Banyak zat berbentuk gas, yang ada di alam dan diperoleh dalam produksi, merupakan senyawa beracun yang kuat. Diketahui bahwa klorin digunakan sebagai senjata biologis, uap brom mempunyai efek yang sangat korosif pada kulit, hidrogen sulfida menyebabkan keracunan, dan sebagainya.
Salah satu zat tersebut adalah karbon monoksida atau karbon monoksida yang rumusannya memiliki ciri struktur tersendiri. Tentang dia dan kita akan bicara lebih jauh.
Rumus kimia karbon monoksida
Bentuk empiris rumus senyawa yang dimaksud adalah sebagai berikut: CO. Namun, bentuk ini hanya mencirikan komposisi kualitatif dan kuantitatif, tetapi tidak mempengaruhi ciri struktural dan urutan ikatan atom dalam suatu molekul. Dan ini berbeda dengan gas serupa lainnya.
Ciri inilah yang mempengaruhi sifat fisik dan kimia yang ditunjukkan oleh senyawa tersebut. Struktur macam apa ini?
Struktur molekul
Pertama, rumus empiris menunjukkan bahwa valensi karbon dalam senyawa adalah II. Sama halnya dengan oksigen. Akibatnya, masing-masing dapat membentuk dua formula karbon monoksida CO, yang dengan jelas menegaskan hal ini.
Inilah yang terjadi. Antara atom karbon dan oksigen, menurut mekanisme pembagian elektron tidak berpasangan, terbentuk ikatan polar kovalen ganda. Jadi, karbon monoksida berbentuk C=O.
Namun, ciri-ciri molekul tidak berakhir di situ. Menurut mekanisme donor-akseptor, ikatan ketiga, datif atau semipolar terbentuk dalam molekul. Apa yang menjelaskan hal ini? Karena setelah pembentukan menurut urutan pertukaran, oksigen memiliki dua pasang elektron, dan atom karbon memiliki orbital kosong, atom karbon bertindak sebagai akseptor salah satu pasangan elektron. Dengan kata lain, sepasang elektron oksigen ditempatkan pada orbital karbon kosong dan ikatan terbentuk.

Jadi, karbon adalah akseptor, oksigen adalah donor. Oleh karena itu, rumus karbon monoksida dalam kimia diambil tampilan selanjutnya: C≡O. Strukturisasi ini memberikan stabilitas kimia tambahan dan kelembaman pada molekul dalam sifat-sifat yang ditunjukkannya dalam kondisi normal.
Jadi, ikatan pada molekul karbon monoksida adalah:
- dua kutub kovalen, dibentuk melalui mekanisme pertukaran karena pembagian elektron yang tidak berpasangan;
- satu datif, dibentuk oleh interaksi donor-akseptor antara sepasang elektron dan orbital bebas;
- Ada total tiga ikatan dalam molekul.
Properti fisik
Ada sejumlah karakteristik yang dimiliki karbon monoksida, seperti senyawa lainnya. Rumus zat memperjelas hal itu sel kristal molekuler, keadaan gas dalam kondisi normal. Parameter fisik berikut mengikuti dari ini.
- C≡O - karbon monoksida (rumus), kepadatan - 1,164 kg/m 3.
- Titik didih dan titik leleh masing-masing: 191/205 0 C.
- Larut dalam: air (sedikit), eter, benzena, alkohol, kloroform.
- Tidak ada rasa atau bau.
- Tanpa warna.
Dari sudut pandang biologis, ini sangat berbahaya bagi semua makhluk hidup kecuali tipe tertentu bakteri.

Sifat kimia
Dari sudut pandang aktivitas kimia, salah satu zat paling lembam dalam kondisi normal adalah karbon monoksida. Rumusnya, yang mencerminkan semua ikatan dalam molekul, menegaskan hal ini. Justru karena strukturnya yang begitu kuat maka senyawa ini menjadi indikator standar lingkungan praktis tidak melakukan interaksi apa pun.
Namun, jika sistem dipanaskan setidaknya sedikit, ikatan datif dalam molekul akan terurai, seperti halnya ikatan kovalen. Kemudian karbon monoksida mulai menunjukkan aktivitas aktif sifat restoratif, dan cukup kuat. Jadi, ia dapat berinteraksi dengan:
- oksigen;
- klorin;
- alkali (meleleh);
- dengan oksida logam dan garam;
- dengan belerang;
- sedikit dengan air;
- dengan amonia;
- dengan hidrogen.
Oleh karena itu, seperti disebutkan di atas, sifat-sifat karbon monoksida sebagian besar dijelaskan oleh rumusnya.

Berada di alam
Sumber utama CO di atmosfer bumi adalah kebakaran hutan. Lagipula cara utama pembentukan gas ini tentu saja- ini adalah pembakaran tidak sempurna berbagai jenis bahan bakar, terutama yang bersifat organik.
Sumber polusi udara antropogenik dengan karbon monoksida juga penting dan menyediakan fraksi massa persentase yang sama dengan yang alami. Ini termasuk:
- asap dari pekerjaan pabrik dan pabrik, kompleks metalurgi dan perusahaan industri lainnya;
- gas buang dari mesin pembakaran dalam.
DI DALAM kondisi alam karbon monoksida mudah teroksidasi oleh oksigen udara dan uap air karbon dioksida. Inilah dasar pertolongan pertama jika terjadi keracunan senyawa ini.

Kuitansi
Perlu diperhatikan satu fitur. Karbon monoksida (rumus), karbon dioksida (struktur molekul) masing-masing terlihat seperti ini: C≡O dan O=C=O. Perbedaannya adalah satu atom oksigen. Oleh karena itu, metode industri untuk menghasilkan monoksida didasarkan pada reaksi antara dioksida dan batubara: CO 2 + C = 2CO. Ini adalah metode paling sederhana dan paling umum untuk mensintesis senyawa ini.
Laboratorium menggunakan berbagai macam senyawa organik, garam logam dan zat kompleks, karena hasil produk diperkirakan tidak terlalu besar.
Reagen berkualitas tinggi untuk mengetahui keberadaan karbon monoksida di udara atau larutan adalah paladium klorida. Ketika mereka berinteraksi, logam murni terbentuk, yang menyebabkan larutan atau permukaan kertas menjadi gelap.

Efek biologis pada tubuh
Seperti disebutkan di atas, karbon monoksida adalah hama yang sangat beracun, tidak berwarna, berbahaya dan mematikan tubuh manusia. Dan bukan hanya manusia, tapi semua makhluk hidup pada umumnya. Tanaman yang terkena knalpot mobil akan cepat mati.
Apa sebenarnya dampak biologis karbon monoksida terhadap lingkungan internal hewan? Ini semua tentang pembentukan senyawa kompleks yang kuat dari protein darah, hemoglobin, dan gas yang dimaksud. Artinya, alih-alih oksigen, molekul racun malah ditangkap. Respirasi seluler langsung diblokir, pertukaran gas menjadi tidak mungkin dilakukan secara normal.
Akibatnya, terjadi pemblokiran bertahap semua molekul hemoglobin dan, akibatnya, kematian. Hanya 80% kerusakan yang cukup untuk membuat keracunan menjadi fatal. Untuk melakukan ini, konsentrasi karbon monoksida di udara harus 0,1%.
Tanda-tanda pertama yang dapat menentukan timbulnya keracunan senyawa ini adalah:
- sakit kepala;
- pusing;
- penurunan kesadaran.
Pertolongan pertama adalah pergi ke udara segar, di mana karbon monoksida di bawah pengaruh oksigen akan berubah menjadi karbon dioksida, yaitu dinetralkan. Kasus kematian akibat aksi zat tersebut sangat sering terjadi, terutama di rumah-rumah dengan pembakaran kayu, batu bara dan jenis bahan bakar lainnya, gas ini tentu akan terbentuk sebagai produk sampingan. Kepatuhan terhadap peraturan keselamatan sangat penting untuk menjaga kehidupan dan kesehatan manusia.
Ada juga banyak kasus keracunan di garasi, di mana banyak mesin mobil yang berfungsi dikumpulkan, tetapi pasokan udara segar tidak mencukupi. Kematian jika terlampaui konsentrasi yang diizinkan datang dalam satu jam. Keberadaan gas secara fisik tidak mungkin dirasakan karena tidak berbau dan tidak berwarna.

Penggunaan industri
Selain itu, karbon monoksida digunakan:
- untuk mengolah daging dan produk ikan, yang memungkinkan Anda memberikan tampilan segar;
- untuk sintesis senyawa organik tertentu;
- sebagai komponen gas generator.
Oleh karena itu, zat ini tidak hanya merugikan dan berbahaya, tetapi juga sangat bermanfaat bagi manusia dan kegiatan perekonomiannya.
Sifat fisik karbon monoksida (karbon monoksida CO) normal tekanan atmosfir tergantung pada suhu pada nilai negatif dan positif.
Dalam tabel Sifat fisik CO berikut disajikan: kepadatan karbon monoksida ρ , panas spesifik pada tekanan konstan C hal, koefisien konduktivitas termal λ dan viskositas dinamis μ .
Tabel pertama menunjukkan densitas dan kapasitas panas spesifik karbon monoksida CO pada kisaran suhu -73 hingga 2727°C.
Tabel kedua memberikan nilai sifat fisik karbon monoksida seperti konduktivitas termal dan viskositas dinamisnya dalam kisaran suhu dari minus 200 hingga 1000°C.
Kepadatan karbon monoksida, seperti , sangat bergantung pada suhu - ketika karbon monoksida CO dipanaskan, kepadatannya menurun. Misalnya, pada suhu kamar massa jenis karbon monoksida adalah 1,129 kg/m3, tetapi dalam proses pemanasan hingga suhu 1000°C, massa jenis gas ini berkurang 4,2 kali lipat - menjadi 0,268 kg/m 3.
Pada kondisi normal(suhu 0°C) karbon monoksida memiliki massa jenis 1,25 kg/m 3. Jika kita membandingkan massa jenisnya dengan gas umum lainnya, maka massa jenis karbon monoksida relatif terhadap udara adalah nilai yang lebih rendah- Karbon monoksida lebih ringan dari udara. Ia juga lebih ringan dari argon, namun lebih berat dari nitrogen, hidrogen, helium dan gas ringan lainnya.
Panas jenis karbon monoksida dalam kondisi normal adalah 1040 J/(kg derajat). Ketika suhu gas ini meningkat, kapasitas panas spesifiknya meningkat. Misalnya, pada 2727°C nilainya adalah 1329 J/(kg derajat).
| t, °С | ρ, kg/m3 | C p , J/(kg derajat) | t, °С | ρ, kg/m3 | C p , J/(kg derajat) | t, °С | ρ, kg/m3 | C p , J/(kg derajat) |
|---|---|---|---|---|---|---|---|---|
| -73 | 1,689 | 1045 | 157 | 0,783 | 1053 | 1227 | 0,224 | 1258 |
| -53 | 1,534 | 1044 | 200 | 0,723 | 1058 | 1327 | 0,21 | 1267 |
| -33 | 1,406 | 1043 | 257 | 0,635 | 1071 | 1427 | 0,198 | 1275 |
| -13 | 1,297 | 1043 | 300 | 0,596 | 1080 | 1527 | 0,187 | 1283 |
| -3 | 1,249 | 1043 | 357 | 0,535 | 1095 | 1627 | 0,177 | 1289 |
| 0 | 1,25 | 1040 | 400 | 0,508 | 1106 | 1727 | 0,168 | 1295 |
| 7 | 1,204 | 1042 | 457 | 0,461 | 1122 | 1827 | 0,16 | 1299 |
| 17 | 1,162 | 1043 | 500 | 0,442 | 1132 | 1927 | 0,153 | 1304 |
| 27 | 1,123 | 1043 | 577 | 0,396 | 1152 | 2027 | 0,147 | 1308 |
| 37 | 1,087 | 1043 | 627 | 0,374 | 1164 | 2127 | 0,14 | 1312 |
| 47 | 1,053 | 1043 | 677 | 0,354 | 1175 | 2227 | 0,134 | 1315 |
| 57 | 1,021 | 1044 | 727 | 0,337 | 1185 | 2327 | 0,129 | 1319 |
| 67 | 0,991 | 1044 | 827 | 0,306 | 1204 | 2427 | 0,125 | 1322 |
| 77 | 0,952 | 1045 | 927 | 0,281 | 1221 | 2527 | 0,12 | 1324 |
| 87 | 0,936 | 1045 | 1027 | 0,259 | 1235 | 2627 | 0,116 | 1327 |
| 100 | 0,916 | 1045 | 1127 | 0,241 | 1247 | 2727 | 0,112 | 1329 |
Konduktivitas termal karbon monoksida dalam kondisi normal adalah 0,02326 W/(m derajat). Nilai ini meningkat seiring meningkatnya suhu dan pada 1000°C menjadi sama dengan 0,0806 W/(m derajat). Perlu dicatat bahwa konduktivitas termal karbon monoksida sedikit lebih kecil dari nilai y ini.
Viskositas dinamis karbon monoksida pada suhu kamar adalah 0,0246·10 -7 Pa·s. Ketika karbon monoksida dipanaskan, viskositasnya meningkat. Jenis ketergantungan viskositas dinamis pada suhu diamati pada . Perlu diperhatikan bahwa karbon monoksida lebih kental dibandingkan uap air dan karbon dioksida CO 2, namun memiliki viskositas yang lebih rendah dibandingkan dengan nitrogen oksida NO dan udara.
Setiap orang yang pernah berurusan dengan pengoperasian sistem pemanas - kompor, ketel uap, ketel uap, pemanas air, yang dirancang untuk bahan bakar rumah tangga dalam bentuk apa pun - tahu betapa berbahayanya karbon monoksida bagi manusia. Cukup sulit untuk menetralisirnya dalam bentuk gas; tidak ada pengobatan rumahan yang efektif untuk melawannya. karbon monoksida tidak ada, jadi kebanyakan tindakan perlindungan ditujukan untuk mencegah dan mendeteksi asap di udara secara tepat waktu.
Sifat-sifat zat beracun
Tidak ada yang aneh dengan sifat dan sifat karbon monoksida. Pada dasarnya, ini adalah produk oksidasi parsial batubara atau bahan bakar yang mengandung batubara. Rumus karbon monoksida sederhana dan jelas - CO, dalam istilah kimia - karbon monoksida. Satu atom karbon terhubung ke atom oksigen. Sifat proses pembakaran bahan bakar organik sedemikian rupa sehingga karbon monoksida merupakan bagian integral dari setiap nyala api.

Ketika dipanaskan di dalam tungku, batu bara, bahan bakar terkait, gambut, dan kayu bakar diubah menjadi gasifikasi menjadi karbon monoksida, dan baru kemudian dibakar bersama aliran udara. Jika karbondioksida bocor dari ruang bakar ke dalam ruangan, maka akan tetap dalam keadaan stabil sampai aliran karbon dikeluarkan dari ruangan melalui ventilasi atau terakumulasi, memenuhi seluruh ruangan, dari lantai hingga langit-langit. Dalam kasus terakhir, hanya sensor karbon monoksida elektronik yang dapat menyelamatkan situasi dengan merespons sedikit pun peningkatan konsentrasi asap beracun di atmosfer ruangan.
Apa yang perlu Anda ketahui tentang karbon monoksida:
- DI DALAM kondisi standar massa jenis karbon monoksida adalah 1,25 kg/m 3, yang sangat dekat dengan berat jenis udara 1,25 kg/m 3. Monoksida panas dan bahkan hangat dengan mudah naik ke langit-langit, dan saat mendingin, ia mengendap dan bercampur dengan udara;
- Karbon monoksida tidak berasa, tidak berwarna dan tidak berbau, bahkan dalam konsentrasi tinggi;
- Untuk memulai pembentukan karbon monoksida, cukup memanaskan logam yang bersentuhan dengan karbon hingga suhu 400-500 o C;
- Gas tersebut mampu terbakar di udara, melepaskannya jumlah besar panas, sekitar 111 kJ/mol.
Tidak hanya menghirup karbon monoksida yang berbahaya, campuran gas-udara juga dapat meledak ketika konsentrasi volume mencapai 12,5% hingga 74%. Dalam hal ini, campuran gas tersebut mirip dengan metana rumah tangga, namun jauh lebih berbahaya daripada gas jaringan.

Metana lebih ringan dari udara dan kurang beracun jika dihirup, selain itu, berkat zat aditif di dalamnya aliran gas bahan tambahan khusus - merkaptan, keberadaannya di dalam ruangan mudah dideteksi dari baunya. Jika dapur sedikit tercemar, Anda dapat memasuki ruangan dan memberikan ventilasi tanpa konsekuensi kesehatan apa pun.
Dengan karbon monoksida, segalanya menjadi lebih rumit. Hubungan erat antara CO dan udara mencegah penghilangan awan gas beracun secara efektif. Saat mendingin, awan gas secara bertahap akan mengendap di area lantai. Jika detektor karbon monoksida terpicu, atau kebocoran produk pembakaran terdeteksi dari kompor atau ketel bahan bakar padat, tindakan ventilasi harus segera diambil, jika tidak, anak-anak dan hewan peliharaan akan menjadi yang pertama menderita.
Sifat serupa dari karbon monoksida sebelumnya banyak digunakan untuk memerangi hewan pengerat dan kecoa, namun efektif serangan gas jauh lebih rendah sarana modern, dan risiko keracunan jauh lebih tinggi.
Untuk informasi anda! Awan gas CO, jika tidak ada ventilasi, dapat mempertahankan sifat-sifatnya tidak berubah untuk waktu yang lama.
Jika diduga terjadi penumpukan karbon monoksida di basement, ruang utilitas, ruang boiler, ruang bawah tanah, langkah pertama yang harus dilakukan adalah memastikan ventilasi maksimal dengan laju pertukaran gas 3-4 unit per jam.
Kondisi munculnya asap di dalam ruangan
Karbon monoksida dapat diproduksi dengan menggunakan banyak pilihan reaksi kimia, tetapi hal ini memerlukan reagen dan kondisi khusus untuk interaksinya. Risiko keracunan gas dengan cara ini hampir sama sama dengan nol. Alasan utama munculnya karbon monoksida di ruang ketel atau area dapur adalah dua faktor:
- Draf yang buruk dan aliran sebagian produk pembakaran dari sumber pembakaran ke area dapur;
- Pengoperasian peralatan boiler, gas dan tungku yang tidak tepat;
- Kebakaran dan kebakaran lokal pada plastik, kabel, lapisan dan bahan polimer;
- Gas buang dari saluran pembuangan.
Sumber karbon monoksida dapat berupa pembakaran sekunder abu, endapan jelaga yang lepas di cerobong asap, jelaga dan resin yang tertanam di dinding bata perapian dan alat pemadam jelaga.

Paling sering, sumber gas CO adalah batu bara yang membara, yang terbakar di tungku ketika katup ditutup. Terutama banyak gas yang dilepaskan selama dekomposisi termal kayu bakar tanpa adanya udara; sekitar setengah dari awan gas ditempati oleh karbon monoksida. Oleh karena itu, setiap percobaan pengasapan daging dan ikan menggunakan kabut yang diperoleh dari serutan yang membara sebaiknya dilakukan hanya di udara terbuka.
Sejumlah kecil karbon monoksida juga mungkin muncul selama memasak. Misalnya, siapa pun yang pernah menemukan pemasangan boiler pemanas gas dengan tungku tertutup di dapur pasti tahu bagaimana sensor karbon monoksida bereaksi terhadap kentang goreng atau makanan apa pun yang dimasak dengan minyak mendidih.

Sifat berbahaya dari karbon monoksida
Bahaya utama karbon monoksida adalah mustahil untuk merasakan dan merasakan keberadaannya di atmosfer suatu ruangan sampai gas tersebut masuk ke sistem pernapasan bersama udara dan larut dalam darah.

Akibat menghirup CO bergantung pada konsentrasi gas di udara dan lama tinggal di dalam ruangan:
- Sakit kepala, malaise dan timbulnya keadaan mengantuk dimulai ketika kandungan volumetrik gas di udara 0,009-0,011%. Secara fisik pria sehat mampu bertahan hingga tiga jam terpapar atmosfer yang tercemar;
- Mual, rasa sakit yang kuat pada otot, kram, pingsan, kehilangan orientasi dapat terjadi pada konsentrasi 0,065-0,07%. Waktu yang dihabiskan di dalam ruangan sampai timbulnya akibat yang tak terhindarkan hanya 1,5-2 jam;
- Ketika konsentrasi karbon monoksida di atas 0,5%, tinggal beberapa detik di ruangan yang tercemar gas berarti kematian.

Bahkan jika seseorang telah melarikan diri dengan selamat dari ruangan dengan konsentrasi karbon monoksida yang tinggi, dia tetap membutuhkannya kesehatan dan penggunaan obat penawar, karena akibat keracunan sistem peredaran darah dan gangguan peredaran darah di otak akan tetap muncul, hanya beberapa saat kemudian.
Molekul karbon monoksida mudah diserap oleh air dan larutan garam. Oleh karena itu, handuk dan serbet biasa yang dibasahi dengan air sering kali digunakan sebagai alat perlindungan pertama. Hal ini memungkinkan Anda menghentikan karbon monoksida memasuki tubuh Anda selama beberapa menit hingga Anda dapat meninggalkan ruangan.
Sifat karbon monoksida ini sering disalahgunakan oleh beberapa pemilik peralatan pemanas yang memiliki sensor CO bawaan. Saat sensor sensitif terpicu, alih-alih memberi ventilasi pada ruangan, perangkat sering kali hanya ditutup dengan handuk basah. Akibatnya, setelah selusin manipulasi seperti itu, sensor karbon monoksida gagal, dan risiko keracunan meningkat berkali-kali lipat.
Sistem deteksi karbon monoksida teknis
Faktanya, saat ini hanya ada satu cara untuk berhasil memerangi karbon monoksida, yaitu dengan menggunakan perangkat elektronik khusus dan sensor yang mencatat kelebihan konsentrasi CO di dalam ruangan. Tentu saja Anda dapat melakukan sesuatu yang lebih sederhana, misalnya memasang ventilasi yang kuat, seperti yang dilakukan oleh mereka yang suka bersantai di dekat perapian batu bata asli. Tapi di keputusan seperti itu ada risiko keracunan karbon monoksida ketika mengubah arah aliran udara di dalam pipa, selain itu, hidup di bawah aliran udara yang kuat juga tidak terlalu baik untuk kesehatan.

Perangkat sensor karbon monoksida
Masalah pengendalian kandungan karbon monoksida di atmosfer perumahan dan ruang utilitas saat ini sama mendesaknya dengan keberadaan alarm kebakaran atau keamanan.
Di toko khusus peralatan pemanas dan gas, Anda dapat membeli beberapa opsi untuk perangkat pemantauan kandungan gas:
- Alarm kimia;
- Pemindai inframerah;
- Sensor keadaan padat.
Sensor sensitif perangkat biasanya dilengkapi dengan papan elektronik yang menyediakan daya, kalibrasi, dan konversi sinyal menjadi bentuk yang jelas indikasi. Ini bisa berupa LED hijau dan merah pada panel, sirene yang dapat didengar, informasi digital untuk mengeluarkan sinyal jaringan komputer atau pulsa kontrol untuk katup otomatis yang mematikan pasokan gas domestik ke boiler pemanas.

Jelas bahwa penggunaan sensor dengan katup penutup yang terkontrol merupakan tindakan yang perlu, tetapi seringkali dilakukan oleh produsen peralatan pemanas sengaja membangun “pelindung yang sangat mudah” untuk menghindari segala macam manipulasi terhadap keamanan peralatan gas.
Instrumen kontrol kimia dan solid state
Versi termurah dan paling terjangkau dari sensor dengan indikator kimia dibuat dalam bentuk labu jaring, mudah ditembus udara. Di dalam labu terdapat dua elektroda yang dipisahkan oleh partisi berpori yang diresapi dengan larutan alkali. Munculnya karbon monoksida menyebabkan karbonisasi elektrolit, konduktivitas sensor turun tajam, yang segera dibaca oleh elektronik sebagai sinyal alarm. Setelah pemasangan, perangkat dalam keadaan tidak aktif dan tidak akan beroperasi hingga terdapat sisa karbon monoksida di udara yang melebihi konsentrasi yang diizinkan.
Sensor solid-state menggunakan kantong dua lapis timah dioksida dan rutenium sebagai pengganti asbes yang diresapi alkali. Munculnya gas di udara menyebabkan putusnya kontak perangkat sensor dan secara otomatis memicu alarm.

Pemindai dan penjaga elektronik
Sensor inframerah beroperasi berdasarkan prinsip memindai udara sekitar. Sensor inframerah internal mendeteksi cahaya LED laser, dan perangkat pemicu diaktifkan berdasarkan perubahan intensitas penyerapan radiasi termal oleh gas.

CO menyerap bagian termal dari spektrum dengan sangat baik, sehingga perangkat tersebut beroperasi dalam mode penjaga atau pemindai. Hasil pemindaian dapat ditampilkan dalam bentuk sinyal dua warna atau indikasi jumlah karbon monoksida di udara dalam skala digital atau linier.
Sensor mana yang lebih baik
Untuk memilih sensor karbon monoksida yang tepat, perlu mempertimbangkan mode pengoperasian dan sifat ruangan tempat perangkat sensor akan dipasang. Misalnya, sensor kimia, yang dianggap ketinggalan jaman, berfungsi dengan baik di ruang ketel dan ruang utilitas. Alat pendeteksi karbon monoksida yang murah dapat dipasang di rumah atau bengkel Anda. Di dapur, jaring dengan cepat tertutup debu dan timbunan lemak, yang secara drastis mengurangi sensitivitas kerucut kimia.
Sensor karbon monoksida keadaan padat bekerja dengan baik di segala kondisi, namun memerlukan sumber daya eksternal yang kuat untuk beroperasi. Biaya perangkat lebih tinggi dari harga sistem sensor kimia.

Sensor inframerah adalah yang paling umum saat ini. Mereka secara aktif digunakan untuk melengkapi sistem keamanan boiler pemanas individu perumahan. Pada saat yang sama, sensitivitas sistem kontrol praktis tidak berubah seiring waktu karena debu atau suhu udara. Selain itu, sistem seperti itu, biasanya, memiliki mekanisme pengujian dan kalibrasi bawaan, yang memungkinkan Anda memeriksa kinerjanya secara berkala.
Pemasangan alat pemantau karbon monoksida
Sensor karbon monoksida harus dipasang dan dirawat secara eksklusif oleh personel yang berkualifikasi. Secara berkala, instrumen harus diperiksa, dikalibrasi, dirawat, dan diganti.
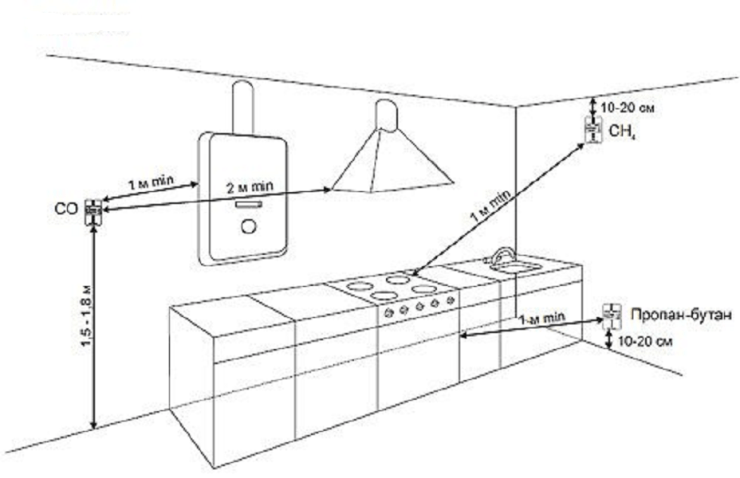
Sensor harus dipasang pada jarak 1 sampai 4 m dari sumber gas; housing atau sensor jarak jauh dipasang pada ketinggian 150 cm di atas permukaan lantai dan harus dikalibrasi sesuai dengan ambang sensitivitas atas dan bawah.
Masa pakai detektor karbon monoksida perumahan adalah 5 tahun.
Kesimpulan
Perjuangan melawan pembentukan karbon monoksida membutuhkan kehati-hatian dan sikap bertanggung jawab terhadap peralatan yang dipasang. Eksperimen apa pun dengan sensor, terutama semikonduktor, secara tajam mengurangi sensitivitas perangkat, yang pada akhirnya menyebabkan peningkatan kandungan karbon monoksida di atmosfer dapur dan seluruh apartemen, yang secara perlahan meracuni seluruh penghuninya. Masalah pemantauan karbon monoksida sangat serius sehingga penggunaan sensor di masa depan mungkin diwajibkan untuk semua kategori pemanasan individu.
Karbon oksida
Tahun-tahun terakhir V ilmu pedagogi Pembelajaran yang berorientasi pada pribadi lebih diutamakan. Pembentukan kualitas individu kepribadian terjadi dalam proses kegiatan: belajar, bermain, bekerja. Oleh karena itu, faktor penting dalam pembelajaran adalah pengorganisasian proses pembelajaran, sifat hubungan antara guru dengan siswa dan siswa satu sama lain. Berdasarkan ide-ide tersebut, saya mencoba membangun proses pendidikan secara khusus. Pada saat yang sama, setiap siswa memilih kecepatannya sendiri dalam mempelajari materi, memiliki kesempatan untuk bekerja pada tingkat yang dapat diakses olehnya, dalam situasi sukses. Selama pembelajaran, dimungkinkan untuk menguasai dan meningkatkan tidak hanya keterampilan khusus mata pelajaran, tetapi juga keterampilan pendidikan umum seperti menetapkan tujuan pendidikan, memilih cara dan cara untuk mencapainya, memantau pencapaian seseorang, dan memperbaiki kesalahan. Siswa belajar bekerja dengan sastra, membuat catatan, diagram, gambar, bekerja dalam kelompok, berpasangan, individu, melakukan pertukaran pendapat yang konstruktif, menalar secara logis dan menarik kesimpulan.
Melaksanakan pembelajaran seperti itu memang tidak mudah, namun jika berhasil maka kepuasan akan terasa. Saya menawarkan naskah untuk salah satu pelajaran saya. Dihadiri oleh rekan-rekan, administrasi dan psikolog.
Jenis pelajaran. Mempelajari materi baru.
Sasaran. Berdasarkan motivasi dan aktualisasi latar belakang pengetahuan dan keterampilan siswa untuk mempertimbangkan struktur, sifat fisik dan kimia, produksi dan penggunaan karbon dioksida dan karbon dioksida.
Artikel ini disiapkan dengan dukungan situs www.Artifex.Ru. Jika Anda memutuskan untuk memperluas pengetahuan Anda di bidang tersebut seni kontemporer, maka solusi terbaik adalah dengan mengunjungi website www.Artifex.Ru. Almanak kreatif ARTIFEX akan memungkinkan Anda mengenal karya seni kontemporer tanpa harus meninggalkan rumah. Lagi Informasi rinci Anda dapat menemukannya di situs web www.Artifex.Ru. Tidak ada kata terlambat untuk mulai memperluas wawasan dan rasa keindahan.
Peralatan dan reagen. Kartu “Survei terprogram”, diagram poster, alat untuk menghasilkan gas, gelas, tabung reaksi, alat pemadam api, korek api; air kapur, natrium oksida, kapur, asam klorida, larutan indikator, H 2 SO 4 (conc.), HCOOH, Fe 2 O 3.
Diagram poster
“Struktur molekul karbon monoksida (karbon monoksida (II)) CO”
SELAMA KELAS
Meja siswa di kantor disusun melingkar. Guru dan siswa mempunyai kesempatan untuk leluasa berpindah ke meja laboratorium (1, 2, 3). Selama pembelajaran, anak-anak duduk di meja belajar (4, 5, 6, 7, ...) satu sama lain sesuai keinginan (kelompok bebas 4 orang).

Guru. Pepatah Cina yang bijak(ditulis dengan indah di papan tulis) membaca:
“Saya mendengar - saya lupa,
Saya mengerti - saya ingat
Ya - saya mengerti.”
Apakah Anda setuju dengan kesimpulan orang bijak Tiongkok?
Peribahasa Rusia apa yang mencerminkan kebijaksanaan Tiongkok?
Anak-anak memberi contoh.
Guru. Memang, hanya dengan berkreasi Anda bisa memperoleh produk yang berharga: zat baru, instrumen, mesin, serta nilai tidak berwujud - kesimpulan, generalisasi, kesimpulan. Saya mengundang Anda hari ini untuk mengambil bagian dalam studi tentang sifat-sifat dua zat. Diketahui, saat menjalani pemeriksaan teknis mobil, pengemudi memberikan surat keterangan tentang kondisi gas buang mobil. Berapa konsentrasi gas yang ditunjukkan dalam sertifikat?
(O t v e t. JADI.)
Murid. Gas ini beracun. Begitu berada di dalam darah, ia menyebabkan keracunan pada tubuh (“terbakar”, oleh karena itu nama oksidanya - karbon monoksida). Hal ini ditemukan dalam gas buang mobil dalam jumlah yang berbahaya bagi kehidupan.(membaca laporan dari surat kabar tentang seorang pengemudi yang tertidur di garasi saat mesin hidup dan meninggal dunia). Penangkal keracunan karbon monoksida adalah menghirup udara segar dan oksigen murni. Karbon monoksida lainnya adalah karbon dioksida.
Guru. Ada kartu “Survei Terprogram” di meja Anda. Biasakan diri Anda dengan isinya dan, pada selembar kertas kosong, tandai jumlah tugas yang Anda tahu jawabannya berdasarkan kemampuan Anda. pengalaman hidup. Di seberang nomor pernyataan tugas, tuliskan rumus karbon monoksida yang terkait dengan pernyataan ini.
Konsultan mahasiswa (2 orang) mengumpulkan lembar jawaban dan berdasarkan hasil jawaban membentuk kelompok baru untuk pekerjaan selanjutnya.
Survei terprogram “Karbon oksida”
1. Molekul oksida ini terdiri dari satu atom karbon dan satu atom oksigen.
2. Ikatan antar atom dalam suatu molekul bersifat kovalen polar.
3. Gas yang praktis tidak larut dalam air.
4. Molekul oksida ini mengandung satu atom karbon dan dua atom oksigen.
5. Tidak berbau atau berwarna.
6. Gas larut dalam air.
7. Tidak mencair bahkan pada suhu –190 °C ( T kip = –191,5 °C).
8. Oksida asam.
9. Ia mudah dikompresi, pada suhu 20 °C di bawah tekanan 58,5 atm menjadi cair dan mengeras menjadi “es kering”.
10. Tidak beracun.
11. Tidak membentuk garam.
12. Mudah terbakar
13. Berinteraksi dengan air.
14. Berinteraksi dengan oksida basa.
15. Bereaksi dengan oksida logam, mereduksi logam bebas darinya.
16. Diperoleh dengan mereaksikan asam dengan garam asam karbonat.
17. SAYA.
18. Berinteraksi dengan alkali.
19. Sumber karbon yang diserap tanaman di rumah kaca dan rumah kaca menyebabkan peningkatan hasil.
20. Digunakan untuk mengkarbonasi air dan minuman.
Guru. Tinjau kembali isi kartu itu. Kelompokkan informasi menjadi 4 blok:
struktur,
properti fisik,
Sifat kimia,
menerima.
Guru memberikan kesempatan kepada setiap kelompok siswa untuk berbicara dan merangkum hasil presentasi. Kemudian siswa kelompok yang berbeda pilih rencana kerja Anda - urutan mempelajari oksida. Untuk tujuan ini, mereka memberi nomor pada blok informasi dan membenarkan pilihan mereka. Urutan pembelajarannya bisa seperti yang tertulis di atas, atau dengan kombinasi lain dari empat blok yang ditandai.
Guru mengarahkan perhatian siswa pada poin-poin penting dari topik tersebut. Karena karbon oksida adalah zat gas, maka harus ditangani dengan hati-hati (instruksi keselamatan). Guru menyetujui rencana untuk setiap kelompok dan menugaskan konsultan (siswa yang telah dipersiapkan sebelumnya).
Eksperimen demonstrasi
1. Menuangkan karbon dioksida dari gelas ke gelas.
2. Memadamkan lilin di dalam gelas saat CO 2 terakumulasi.
3. Tempatkan beberapa potong kecil es kering ke dalam segelas air. Air akan mendidih dan keluar asap putih kental.
Gas CO 2 sudah dicairkan pada suhu kamar di bawah tekanan 6 MPa. Dalam keadaan cair, disimpan dan diangkut dalam silinder baja. Jika Anda membuka katup silinder seperti itu, cairan CO 2 akan mulai menguap, yang menyebabkan pendinginan yang kuat dan sebagian gas berubah menjadi massa seperti salju - "es kering", yang ditekan dan digunakan untuk menyimpan es krim.
4. Demonstrasi alat pemadam api berbusa kimia (CFO) dan penjelasan prinsip pengoperasiannya menggunakan model – tabung reaksi dengan sumbat dan tabung saluran keluar gas.

Informasi tentang struktur pada tabel No. 1 (kartu instruksi 1 dan 2, struktur molekul CO dan CO 2).
Informasi tentang properti fisik – di meja No. 2 (bekerja dengan buku teks – Gabrielyan O.S. Kimia-9. M.: Bustard, 2002, hal. 134–135).
Data tentang penerimaan dan sifat kimia – pada tabel No. 3 dan 4 (kartu instruksi 3 dan 4, instruksi kerja praktek, hal. 149–150 dari buku teks).
Kerja praktek Masukkan beberapa potong kapur atau marmer ke dalam tabung reaksi dan tambahkan sedikit asam klorida encer. Tutup tabung dengan cepat menggunakan sumbat dan tabung saluran keluar gas. Masukkan ujung tabung ke dalam tabung reaksi lain yang berisi 2–3 ml air kapur. Perhatikan selama beberapa menit saat gelembung gas melewati air kapur. Kemudian keluarkan ujung tabung saluran keluar gas dari larutan dan bilas dengan air suling. Masukkan tabung reaksi ke dalam tabung reaksi lain yang berisi 2-3 ml air suling dan masukkan gas ke dalamnya. Setelah beberapa menit, keluarkan tabung dari larutan dan tambahkan beberapa tetes lakmus biru ke dalam larutan yang dihasilkan. Tuang 2-3 ml larutan natrium hidroksida encer ke dalam tabung reaksi dan tambahkan beberapa tetes fenolftalein ke dalamnya. Kemudian lewati gas melalui larutan. Jawablah pertanyaan. Pertanyaan 1. Apa yang terjadi jika kapur atau marmer diolah asam hidroklorik? 2. Mengapa, ketika karbon dioksida dilewatkan melalui air kapur, larutan mula-mula menjadi keruh, kemudian kapur larut? 3. Apa yang terjadi jika karbon(IV) monoksida dilewatkan melalui air suling? Tulis persamaannya reaksi yang sesuai dalam bentuk ion molekuler, ionik, dan disingkat. Pengenalan karbonat Keempat tabung reaksi yang diberikan kepadamu berisi zat kristal: natrium sulfat, seng klorida, kalium karbonat, natrium silikat. Tentukan zat apa yang ada di setiap tabung reaksi. Tulis persamaan reaksi dalam bentuk molekul, ionik, dan ionik yang disingkat. |
Pekerjaan rumah
Guru menyarankan untuk membawa pulang kartu “Survei Terprogram” dan sebagai persiapan pelajaran berikutnya memikirkan cara untuk memperoleh informasi. (Bagaimana Anda tahu bahwa gas yang Anda pelajari mencair, bereaksi dengan asam, beracun, dll?)
Pekerjaan mandiri siswa
Kerja praktek sekelompok anak tampil bersama pada kecepatan yang berbeda. Oleh karena itu, permainan ditawarkan kepada mereka yang menyelesaikan pekerjaan lebih cepat.
Roda kelima
Keempat zat mempunyai kesamaan, tetapi zat kelima yang menonjol dari rangkaian tersebut, tidak berguna.
1. Karbon, intan, grafit, karbida, karabin. (Karbit.)
2. Antrasit, gambut, kokas, minyak, kaca. (Kaca.)
3. Batu kapur, kapur, marmer, perunggu, kalsit. (Malachite.)
4. Soda kristal, marmer, kalium, kaustik, perunggu. (Pedas.)
5. Fosgen, fosfin, asam hidrosianat, kalium sianida, karbon disulfida. (Fosfin.)
6. Air laut, air mineral, air suling, air tanah, air sadah. (Air sulingan.)
7. Susu jeruk nipis, bulu halus, jeruk nipis, kapur sirih, air jeruk nipis. (Batu gamping.)
8. Li 2 CO 3; (NH 4) 2 BERSAMA 3; CaCO 3; K 2 BERSAMA 3 , Na 2 BERSAMA 3 . (CaCO3.)
Sinonim
Menulis rumus kimia zat atau namanya.
1. Halogen -... (Klorin atau brom.)
2. Magnesit – ... (MgCO 3.)
3. Urea –... ( Urea H 2 NC(O)NH 2 .)
4. Kalium - ... (K 2 CO 3.)
5. Es kering - ... (CO 2.)
6. Hidrogen oksida –... ( Air.)
7. Amonia – … (10% larutan air amonia.)
8. Garam asam sendawa – … (Nitrat– KNO 3, Ca(NO 3) 2, NaNO 3.)
9. Gas alam – … (metana Bab 4.)
Antonim
Tulislah istilah-istilah kimia yang maknanya berlawanan dengan yang diusulkan.
1. Zat pengoksidasi –... ( Agen pereduksi.)
2. Donor elektron –… ( Akseptor elektron.)
3. Sifat asam – … (Properti dasar.)
4. Disosiasi –… ( Asosiasi.)
5. Adsorpsi – ... ( Desorpsi.)
6. Anoda –... ( Katoda.)
7. Anion –… ( Kation.)
8. Logam –… ( Bukan metal.)
9. Zat awal –... ( Produk reaksi.)
Cari pola
Tetapkan suatu tanda yang menggabungkan zat dan fenomena tertentu.
1. Intan, karabin, grafit – ... ( Modifikasi karbon alotropik.)
2. Kaca, semen, batu bata - ... ( Bahan bangunan.)
3. Bernafas, membusuk, letusan gunung berapi - ... ( Proses disertai dengan pelepasan karbon dioksida.)
4. CO, CO 2, CH 4, SiH 4 – ... ( Senyawa unsur golongan IV.)
5. NaHCO 3, CaCO 3, CO 2, H 2 CO 3 – ... ( Senyawa oksigen karbon.)










